ایلنا گزارش میدهد:
«مایفورتیک» داروی بیماران پیوندی کمیاب است+پاسخ سازمان غذا و دارو
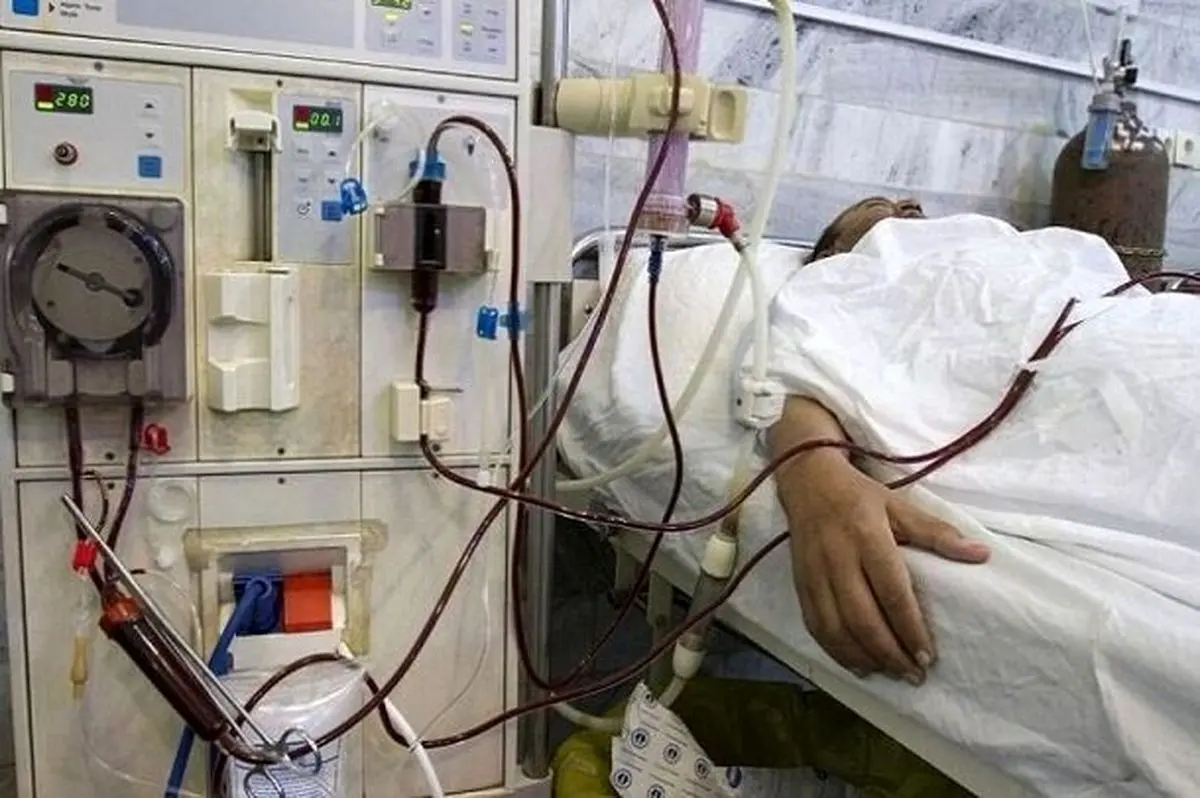
رییس تیم پیوند کبد بیمارستان امام خمینی در واکنش به کمبود «مایفورتیک»؛ داروی وارداتی بیماران پیوندی گفت: نمیتوان گفت که اثربخشی نمونههای داخل کاملا مشابه نمونههای وارداتی است و هیچ گونه تفاوتی با یکدیگر ندارند، اما لازم به ذکر است عموما داروهایی که در کشور استانداردهای لازم جهت تولید را دارند و در بازار موجودند، در فاز بعد از پیوند عضو، قابل استفاده هستند.
یک بیمار پیوندی در پی تماس تلفنی با خبرنگار ایلنا از کمبود داروی مایفورتیک ۳۶۰ خبر داد و گفت: حدود دو ماه است که داروی مایفورتیک کمیاب شده است. تا پیش از آن سهمیه دریافتی ما به اندازه دو ماه بود، اما طی دو ماه اخیر هر زمان که به داروخانه مراجعه میکردیم، تنها به اندازه ۱۵ روز دارو دریافت میکردیم.
او ادامه داد: در حال حاضر نمونه وارداتی داروی مایفورتیک در داروخانهها موجود نیست و گفته میشود که باید نمونه تولید داخلی این دارو مصرف شود. این درحالی است که توصیه پزشکان بر مصرف نمونه خارجی این دارو است، چرا که مصرف نمونه داخلی آن ممکن است، عضو پیوندی را با چالش مواجه کند.
رییس تیم پیوند کبد بیمارستان امام خمینی:
دو تا سه ماه بعد از عمل پیوند داروهای تولید داخل قابل استفادهاند
«علی جعفریان» رییس تیم پیوند کبد بیمارستان امام خمینی در گفتوگو با خبرنگار ایلنا در پاسخ به این سوال که آیا نمونه تولید داخل داروی وارداتی مایفورتیک کارایی و اثر بخشی لازم را برای جایگزینی دارد؟ گفت: نمیتوان گفت که اثربخشی نمونههای داخل کاملا مشابه نمونههای وارداتی است و هیچ گونه تفاوتی با یکدیگر ندارند. اما لازم به ذکر است که عموما داروهایی که در کشور، استانداردهای لازم جهت تولید را دارند و در بازار موجودند، در فاز بعد از پیوند عضو قابل استفاده هستند.
رییس تیم پیوند کبد بیمارستان امام خمینی ادامه داد: در فاز اولیه پس از پیوند عضو از داروی خارجی استفاده میکنیم، چرا که ممکن است داروهای تولید داخل در این مرحله عوارضی را برای بیمار ایجاد کنند، اما وقتی وضعیت بیمار از نظر عملکرد کبد یا هر عضو پیوندی دیگر پایدار شد و دو یا سه ماه از عمل پیوند گذشته است، عموما داروهای تولید داخل قابل استفادهاند و میتوان جایگزین کرد.
رییس سازمان غذا و دارو:
مایفورتیک، مشمول محدودیت واردات است
«حیدر محمدی» رییس سازمان غذا و دارو در خصوص دسترسی دشوار به دارو مایفورتیک به خبرنگار ایلنا توضیح داد: نکتهای که باید در خصوص دشواری دسترسی به هر گونه دارویی در نظر داشت، این است که نمونه تولید داخل اکثر داروها موجود است، اما پزشک و خود بیمار تمایل دارند که نمونه خارجی آن را استفاده کنند. این در حالی است که طبق قانون اگر دارویی در کشور تولید میشود، نمونه مشابه خارجی آن را نمیتوان تجویز کرد و این امر منع قانونی دارد. ما بارها از پزشکان درخواست کردیم، داروهایی را تجویز کنند که در فهرست دارویی یا همان فارماکوپه وجود دارد.
وی ادامه داد: در خصوص داروی مایفورتیک باید در نظر داشت که یک داروی خارجی است و نمونه داخلی آن در کشور به میزان کافی تولید میشود. نمونه تولید داخل این دارو مانند دیگر داروهای تولید داخل، مشمول محدودیت واردات است.
رییس سازمان غذا و دارو متذکر شد: با توجه به اینکه داروی مایفورتیک برای بیماران پیوندی استفاده میشود، لازم است برای بخشی از بیماران که به این دارو نیاز دارند سهمیه تعلق گیرد. لذا سازمان غذا و دارو بر اساس میزانی که معاونت درمان وزارت بهداشت اعلام میکند به این بیماران سهمیه میدهد.
وی تصریح کرد: لازم است تعادلی در توزیع بین نمونه وارداتی داروی مایفورتیک و نمونه تولید داخل آن ایجاد کنیم، به نحوی که به تولید داخل این دارو آسیب نرسد. بیمارانی که مشکلی برای مصرف تولید داخل این دارو ندارند، حتما نمونه تولید داخل را مصرف کنند. چنانچه بیماری به نمونه داخلی عوارض نشان میدهد از نمونه وارداتی آن که برند مایفورتیک است استفاده کند.
مشاور رییس سازمان غذا و دارو:
بیمارانی که نمونه تولید داخل برایشان اثربخش است از آن استفاده کنند
«محمد هاشمی» مشاور رییس سازمان غذا و دارو نیز یادآور شد: تقاضا داریم با توجه به محدودیتهای تامین داروهای خارجی به دلیل محدودیتهای تامین کننده خارجی و محدودیتهای انتقال ارز، افرادی که نمونه تولید داخل برایشان اثربخش و سازگار است از نمونههای تولید داخل استفاده کنند.
سرپرست روابط عمومی سازمان غذا و دارو در پاسخ به سوالی درباره عوارض احتمالی داروی تولید داخل جایگزین مایفورتیک وارداتی گفت: باید در نظر داشت که دارو یک سلسله مراتبی را طی میکند تا مجوز تولید دریافت کند، بنابراین اگر ادعا شود که دارویی موجب بروز عوارض برای بیماران میشود باید از طریق مرکز ثبت و بررسی عوارض ناخواسته داروهای (ADR) سازمان غذا و دارو، اقدام به ارائه گزارش کنند. همکاران ما بررسیهای لازم را انجام میدهند و با توجه به نتیجه مثبت یا منفی گزارش اقدام لازم را انجام میدهند.